高中化学试题
- 将红热的固体单质甲放入久置呈黄色的溶液乙中,剧烈反应产生混合气体A,A在常温下不与空气反应。答案与解析

(1)试推断:甲为________、乙为________、丙为________、
A为________、B为________、C为________。
(2)写出甲与乙反应的化学方程式:_____________________________________。 - 关于乙醇的说法中正确的是( )
- A乙醇结构中有—OH,所以乙醇溶解于水,可以电离出$OH^{-}$而显碱性
- B乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
- C乙醇与钠反应可以产生氢气,所以乙醇显酸性
- D乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
- A
- 物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为$N_{2}O$,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
- A晶体硅熔点高硬度大,可用于制作半导体材料
- B氢氧化铝具有弱碱性,可用于制胃酸中和剂
- C漂白粉在空气中不稳定,可用于漂白纸张
- D氧化铁能与酸反应,可用于制作红色涂料
- A
- 下列物质性质与应用对应关系正确的是()
- A晶体硅熔点高硬度大,可用于制作半导体材料
- B氢氧化铝具有弱碱性,可用于制胃酸中和剂
- C漂白粉在空气中不稳定,可用于漂白纸张
- D氧化铁能与酸反应,可用于制作红色涂料
- A
- 某实验小组用下列装置进行乙醇催化氧化的实验。答案与解析
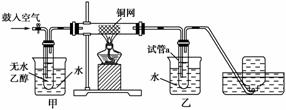
(1)实验过程中铜网出现红色和黑色交替出现的现象,请写出相应的化学反应方程式:
________________________________________________________________________,
________________________________________________________________________。
(2)甲和乙两个水浴作用不相同。
甲的作用是:
乙的作用是:
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________;集气瓶中收集到的气体的主要成分是________________。 - “绿色化学”对化学反应提出了“原子经济性”(原子节约)的概念及要求.理想的原子经济性反应中原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放.以下反应中最符合“绿色化学”的是( )
- A乙烯与氧气在银的催化作用下生成环氧乙烷
- B利用乙烯与HCl反应,制备氯乙烷
- C以苯和液溴为原料,在一定条件下生产溴苯
- D乙醇与浓硫酸共热制备乙烯
- A
- 由乙烯和乙醇组成的混合气体,经测定其中碳元素的质量分数为60%,则混合气体中氧元素的质量分数为( )
- A32.00%
- B20.00%
- C26.67%
- D14.22%
- A
- 丙烯醇($CH_{2}===CH—CH_{2}OH$)可发生的化学反应有( )
①加成 ②氧化 ③燃烧 ④加聚 ⑤取代- A①②③
- B①②③④
- C①②③④⑤
- D①③④
- A
- 等质量的铜片,在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是( )
- A硝酸
- B无水乙醇
- C石灰水
- D盐酸
- A
- 下列说法中正确的是( )
- A醇在Cu或Ag的催化作用下都可以氧化
- B乙醇的分子间脱水反应属于消去反应
- C醇都可以在浓$H_{2}SO_{4}$作用下在170℃时发生消去反应
- D一元饱和脂肪醇的化学式可以用通式$C_{n}H_{2n}$+2O表示
- A
